انواع فتوسنتز در گیاهان
انواع فتوسنتز در گیاهان :
زیست بوم : در گياهان مختلف سبزينه دار كه فتوسنتز انجام مي دهند، ماده غذایی ساخته شده که اولين محصول پايدار می باشد، متفاوت است . بدين معني كه اولين محصول پايدار در دسته اي از گياهان يك اسيد سه كربني به نام «3- فسفو گليسيريك اسيد» و دسته اي ديگر يك اسيد چهار كربني به نام« دي كربوكسيليك اسيد » ( داراي دو عامل كربوكسيل COOH- ، مثل اسيد اگزالواستيك ،اسيد ماليك ، اسيد آسپارتيك ) مي باشد . گياهاني كه اولين محصول پايدار حاصل از فتوسنتز آن ها يك اسيد سه كربنه است گياهان C3 و آندسته كه اولين محصول پايدار آن ها چهار كربني است گياهان C4 ناميده مي شوند . گياهان C4 در مقايسه با گياهان C3 از بازدهي فتوسنتزي بيشتري برخوردارند . بر همين پايه علف هاي هرز C4 نسبت به علف هاي هرز C3 قدرت رقابت زيادتري دارند . در تعدادي از گياهان گوشتي فرآيند فتوسنتزي ديگري مشاهده شده كه در شرايط رطوبت كم روزنه ها در شب باز شده و Co2 جذب مي كنند و در روز بسته مي شوند لذا شدت تعرق گياه خيلي كم مي شود . به اين نوع مكانيسم ، متابوليسم كراسولايي (CAM) "Crassulation asid metabolism" مي گويند مانند آگاو ،آناناس ،كاكتوس . كليه ي گياهان (CAM) جزءگياهان گوشتي غير نمكدوست هستند و عموما با محيط هاي خشك سازگارند .
90% گونه های گیاهی خاکی ، که شامل بخش عظیمی از محصولات گیاهی می باشد ، جز گیاهان C3 هستند مثل برنج ( Oryza sativa) ، گندم ( Triticum aestivum ) ، سویا ( Glycine max) و سیب زمینی ( Solanum tuberosum) . این ها CO2 را به طور مستقیم در مسیر فتوسنتزی C3 اسیمیله می کنند که سیکل کالوین یا سیکل احیاء کربن فتوسنتزی ( PCR ) نامیده می شود. گیاهان C4 و CAM دارای یک مسیر فتو سنتزی منحصر به فرد می باشند و این مسیر به آنها اجازه می دهد تا با شرایط خاص محیطی سازگار بشوند ( 17 ).

1.تثبیت ابتدایی CO2 در سیتوزول سلول های مزوفیل به وسیله فسفو انول پیروات کربوکسیلاز PEPC و تبدیل به اسید C4 یعنی اگزالواستات ( OAA )
2.دکربوکسیلاسیون اسید C4 در سلول های غلاف آوندی و آزاد کردن CO2
3. تولید پذیرنده اولیه CO2 یعنی فسفو انول پیروات PEP یک مولکول CO2 از سیتوزول سلول های مزوفیل به مجاورت روبیسکو در کلروپلاست سلول های غلاف آوندی پمپ می شود و دو مولکول ATP مصرف می شود ( 17 ).
انواع مسیرهای C4
قبل از اینکه C4 صادر می شود ، اگزالواستات به مالات به وسیله آنزیم NADP مالات هیدروژناز یا ( NADP- MDH ) در تیپ NADP- ME احیا می شود و یا توسط آسپارتات آمینوترانسفراز ( AspAT ) در تیپ PEPCK به آسپارتات ترانس آمینه می شود . تولید PEP ( فسفو انول پیروات ) به وسیله پیروات ، ارتوفسفات دی کیناز ( PPDK ) صورت می گیرد ( 7 ، 17 ).
در گونههاي NADP-ME ، اوگزالواستات سريعاً به وسيلة NADPH در كلروپلاست مزوفيل به مالات احيا ميشود. در گونههاي NAD-ME و PEP-CK ، اوگزالواستات در سيتوسول، ترانس آميناسيون ميشود. در واكنش ترانس آميناسيون، گلوتامات به عنوان بخشندة عامل آمينو عمل ميكند. سپس اسيدهاي C4 به سلولهاي غلاف آوندي منتقل ميشوند. در گونه های NADP-ME ، مالات وارد كلروپلاست سلول غلاف آوندي ميشود و دكربوكسيلاسيون بر روي آن صورت ميگيرد در گونه های NAD-ME و PEP-CK ، آسپارتات به سلول غلاف آوندي منتقل ميشود و در وهلة اول، از طريق ترانس آميناسيون، در ميتوكندري (براي گونه های NAD-ME) يا سيتوسول (در گونه های PEP-CK) به اوگزالواستات تبديل ميشود. سپس اوگزالواستات در ميتوكندري گونههاي NAD-ME احيا ميگردد و به وسيلة آنزيم ماليك NAD- ، عمل دكربوكسيلاسيون صورت ميگيرد. اوگزالواستات در سيتوسول گونههاي PEP-CK ، از طريق –PEP كربوكسسيكيناز، دكربوكسيله مي شود. در تمامي اين سه مسير، CO2 آزاد شده در سلول غلاف آوندي، از طريق چرخة PCR به كربوهيدرات تبديل ميشود ( 7 ).
نوع اسيد C3 كه به سلول مزوفيل بر ميگردد نيز بسته به نوع چرخة PCA فرق ميكند. در گونههاي NADP-ME ، اسيد C3 اي كه به مزوفيل ميگردد، پيرووات است، در صورتي كه در دو گونة ديگر احتمالاً آلانين ميباشد. در هر سه نوع چرخه، يك اسيد چهار كربنة دي كربوكسيليك به جاي اسيد سه كربنة مونوكربوكسيليك به سلول غلاف آوندي منتقل ميشود. انتقال اين متابوليتها احتمالاً با حركتهاي جبراني پروتونها و يونهاي ديگري همراه است كه در حفظ pH و توازن بار نقش دارند. در سيتوسول مزوفيل گونه های NAD-ME و PEP-CK ، آلانين از طريق ترانس آميناسون به پيرووات تبديل ميشود. مرحلة نهايي چرخة PCA كه در هر سه نوع چرخه مشترك است، شامل تبديل پيرووات به فسفواينول پيرووات است كه در كلروپلاست مزوفيل صورت ميگيرد. پیرووات ، ارتوفسفات دی کیناز ( PPDK ) Pyruvat , Orthophosphate dikinase یک آنزیم اصلی روزنه ای در اسیمیلاسیون کربن در مسیر فتوسنتزی C4 می باشد. مشابه سایر آنزیم های مسیر های فتوسنتزی مختلف ، این آنزیم نیز منحصرا و به طور قابل برگشت توسط نور ، تنظیم می شود. این تنظیم به پروتئین تنظیم کننده ( RP ) PPDk واگذار شده است ( 12 ، 18 ).
پیروات ارتو فسفات دی کیناز
پیرووات ارتو فسفات دی کیناز (PPDK ) ابتدا در برگ های C4 کشف شد . این یک آنزیم فراوان در کلروپلاست های مزوفیل می باشد که در فتو سنتز C4در گیر است ( 2، 6 ).
C4PPDK و تنظیمش به وسیله عملکرد زیستی تنظیم کننده PPDK
PPDk پیرووات ، ارتوفسفات دی کیناز در گیاهان C4 ، تولید پذیرنده اولیه CO2 یعنی فسفو انول پیرووات PEP را در استرومای کلروپلاست در سلول های مزوفیل برگ کاتالیز می کند . حداکثر فعالیت این آنزیم وقتی است که به صورت هموتترامر با زیرواحدهای تقریبا 95 کیلو دالتونی باشد.وقتی که در دمای سرد invitro باشد به دایمرها و همو دایمر های غیر فعال تبدیل می شود. روی هم رفته مکانیسم کاتالیتیکی پیرووات ، ارتوفسفات دی کیناز PPDK یک کمپلکس است و به آسانی قابل برگشت است. 3 واکنش متوالی قابل برگشت که گسترده اش چنین است : فرم آزاد E – His ، پیروفسفوریل E – His – pp و فسفوریل E –His - p می باشد . بنیان فعال اصلی His می باشد ( شکل 3 ) ( 2 ).

فسفو انول پیروات کربوکسیلاز PEPC ، اولین مرحله از تثبیت دی اکسید کربن فتوسنتزی را کاتالیز می کند.این آنزیم از ارگانیزم های مختلف از جمله گیاهان و باکتری های مختلف ایزوله شده است. تمام فسفو انول کربوکسیلاز های (PEPC ) شناخته شده ، آنزیم های تترامریک با وزن مولکولی 440000 می باشد. سکانس های اسید آمینه این فسفوانول پیروات کربوکسیلاز PEPCها محافظت معنا داری را نشان می دهد. برای مثال ZmPEPC و EcPEPC 40 % برابری کامل دارند ( شکل 5 ).این مطلب نشان می دهد که مکانیسم های واکنشی آنزیم های مختلف برای ارگانیزم های مختلف ، مشابه است. در بسیاری از نمونه ها ، فعالیت آنزیم به صورت آلوستریکی به وسیله گوناگونی اثرات متابولیتی مثبت ( گلوکز 6 – فسفات ) و منفی ( مالات و آسپارتات ) کنترل می شود ( 5 ، 14 ، 19 ).
تنفس نوری
تنفس نوری در گیاهان C3 به علت واکنش رقابتی ریبولوز بیس فسفات کربوکسیلاز / اکسیژناز ( روبیسکو ) می باشد. تنفس نوری کارایی اسیمیلاسیون CO2 را کاهش می دهد و تحت شرایط
محیطی مثل استرس آبی در دمای بالا اتفاق می افتد. در مقابل ، گیاهان C4 یک مسیر CO2 اتمسفری منحصر به فرد دارند که در آن آنزیم فسفو انول پیروات کربوکسیلاز PEPC درگیر می باشد( 14 ، 15 ).
برخلاف روبیسکو فسفو انول پیروات کربوکسیلاز PEPC از HCO3 به جای CO2 به عنوان سوبسترا استفاده می کند.و به طور نسبی میل ترکیبی بالایی برای یون بی کربنات دارد. فسفو انول پیروات کربوکسیلاز PEPC فرم C4 بیشتر از گیاهان C3 بیان می شود.در گیاهان C4 بعد از کربوکسیلاسیون با PEP اسید 4 کربنه به کلروپلاست سلول ها غلاف آوندی فرستاده می شود و روبیسکو عمل دکربوکسیلاسیون را بر روی CO2 تغلیظ شده انجام می دهد. در نتیجه فعالیت اکسیژنازی روبیسکو در گیاهان C4 به طور موثر کاهش می یابد. مکانیسم واکنش فسفو انول پیروات کربوکسیلاز PEPC میل ترکیبی بالایی برای بی کربنات دارد و توسط CO2 مهار نمی شود ( 14 ).
اخیرا آزمایش هایی برای القاء ژن های ویژه C4 در گیاهان C3 صورت گرفته است تا کارایی تثبیت CO2 در سیکل فتوسنتزی C3 از طریق تکنیک های recombinant DNA بهبود یابد. ژن های فسفو انول پیروات کربوکسیلاز PEPC همچنین بیان بالایی در گیاهان C3 مثل برنج ، سیب زمینی و تنباکو دارند . به طور ویژه سطح بالای بیان در گیاهان برنج ترانسژن با فسفو انول پیروات کربوکسیلاز PEPC ذرت ، کاهش مهار فتوسنتز توسط اکسیژن را نشان می دهد. در سیب زمینی های تراریخت ، بیان بالا ( over experesion ) در ژن فسفو انول پیروات کربوکسیلاز PEPC به علت القاء سایر آنزیم های C4 می باشد. حتی فعال سازی فسفو انول پیروات کربوکسیلاز PEPC در گیاهان تراریخت به وسیله متابولیت ها مثل مالات و گلوکز 6 – فسفات کنترل می شود ( 14 ).
ژنهاي مسئول در سنتز فسفو انول پیروات کربوکسیلاز
خانواده ژني PEPC فسفوانول پيرات كربوكسيلاز در Sorghum و ساختار PEPC فسفوانول پيرات كربوكسيلاز مطالعات مولكولي و ژنتيكي مختلفي صورت گرفت و ژنهاي يافت شده در هر كدام از گونهها را زير مشاهده ميكنيد:
1- SVC3 (C3-type house keeping )
2- C4 – type photosynthetic( SVC4 )
3- (C3 type, root inducible( SVC3RI
ژنهاي SVC3 ، SVC3RI و SVC4 داراي 6018 ، 7586 و 7071 نوكلئوتيد ميباشند. و تقريباً 960 اسيد آمينه را به رمز در ميآورند. هر ژن داراي 9 انترون به اندازههاي مختلف است ولي در جايگاههاي مشابه در طول توالي كد كننده قرار گرفتهاند. نقطه شروع رونويسي در SVC4 و SVC3RI به وسيله S1 نوكلئاز در آزمايشهاي محافظتي مشخص شد. در ناحيه N ترمينال پروتئين ، سرينهاي تنظيم كننده وجود دارند و سكانسهاي وابسته به سايتهاي فعال و مهار كننده در انتهاي ناحيه C ترمينال وجود دارد. خانواده ژني PEPC فسفوانول پيرات كربوكسيلاز در تمام گونههاي گياهي و دیگرنيز يافت شد. و يك توافق خوب در زمينه تنوع ايزوزيمهاي PEPC فسفوانول پيرات كربوكسيلاز و نتايج فيزيولوژيكي بدست آمد ( 14 ).
فتوسنتز در گياهان خاكي نياز به ساختار كرانز ندارد.
فتوسنتز C4 ، يك مكانيسم كربن تغليظ شده است كه در گياهان خاكي كه در مناطق با CO2 اتمسفري كم زندگي ميكنند، استفاده ميشود. گياهان C4 با كربوكسيله كردن فسفوانول پيروات PEP ، CO2 را در لايه خارجي سلولهاي مزوفيلي فتوسنتزي متمركز ميكنند. در نتیجه يك اسيد 4 كربنه (C4acid) به سلولهاي لايه bundle sheath (غلاف آوندي)مي رود. در اينجا ريبولوز او 5 بيس فسفات كربوكسيلاز/اكسيژناز (روبيسكو) و واكنشهاي احياي كربن فتوسنتزي (PCR) متمركز شده است. دو لايه از سلولها يك ظاهر حلقوي به ساختار برگ ميدهد كه ساختار كرانز ناميده ميشود. در سلولهاي PCR اسيدهاي C4 جهت توليد CO2 و اسيدهاي آلي 3 كربنه دكربوكسيله ميشوند. اسيد C3 به لايه PCA باز ميگردد تا به فسفوانول پيروات تبديل شود تا CO2 آزاد شده در اطراف روبيسكو انباشته شود و داراي غلظتي بالا باشد تا از تنفس نوري جلوگيري شود ( 13 ، 20 ).
اگرچه فتوسنتز در C4ها هميشه در يك مسير بيوشيميايي مورد بررسي قرار گرفته است ولي دقيقاً بيشتر از 12 تركيب شيميايي و آناتومي شناخته شده كه مستقل از 30 ميليون سال گذشته است. با توجه به اين تنوع ولي تمام گياهان C4 در مرحلة ابتدايي يعنی كربوكسيلاسيون فسفوانول پيروات مشترك هستند و تا اين اواخر تصور ميشد كه ساختار كرانز براي فتوسنتر C4هاي خاكي عضوي ضروري است. 3 مطالعة جديد اين مطلب را به چالش ميكشاند كه آيا ساختار كرانز براي فتوسنتز C4ها ضروري است. اين كه فتوسنتز C4 در chenopods آسيايي مركزي و Borszczowia ardocaspica & Bienertia cycloptera در تك سلولها عمل ميكند ( 20 ).
يك ويژگي مهم، هر مكانيسم كربن تغليظ شده، توانايي آن در انتشار گازهاي محدود شده بيش از ميزان CO2 ميباشد. در جلبكهاي آبزي و بعضي از گياهان آبزي، مكانيسمهاي كربن تغليظ شده در سلولهاي واحد، اتفاق ميافتد، اما در اينجا كمبود مربوط به ماتريكس محيط آبي است كه انتشار گازها را خارج از سلول محدود ميكند. بسياري از جلبك ها، كربن معدني را تغليظ ميكنند. همچنين بعضي از آنژيوسپرم ها (نهاندانگان) Egeria densa و Hydrilla verticillata و دياتومها Thalassiosira weissflogii گزارش شده است كه سيكل فتوسنتزي C4 به طور كامل در سلولهاي فتوسنتزي منفرد انجام ميشود. برخلاف اين وضعيت كه در زيستگاههاي آبي موجود است. در محيطهاي غيرآبي هيچ محدوديتي براي جريان CO2 وجود ندارد. بنابراین تصور ميشد كه تغييري كه باعث جدايي سلولهاي PCR و PCA بود در جهت ايجاد يك عملكرد مؤثر فتوستز C4 در گياهان خاكي بوده است. به طور دقيق ديواره يك مقاومت بالايي در برابر CO2 كم دارد. تا اينكه اجازه ميدهد كه متابوليك سريع بين سلولهاي PCR و PCA از طريق شبكه پلاسمودسماتا برقرار شود. دانستن اين مطالعات و اينكه هر گونه C4 خاكي كه در گذشته مشخص شده، يكي از فرمهاي ساختار كرانز را داد. كشف فتوسنتز C4 در يك سلول يا بدون ساختار كرانز در گياهان خاكي شگفتانگيز است ( 20 ).

Borszcowia arlocasipicaa. سلولهاي فتوسنتزيImmunolocalization روبسيكو در انتهاي پروكسيمال (P)شکل: سلول نشان داده شده با احياي كربن فتوسنتزي (PCR) و كلروپلاستهاي قرمز و پروكسيمال به سمت مكان دستجات آوندي ارجاع داده شده است. پيروات pi-dikinase شامل كروپلاستها [نشان داده شده با اسيميلاسيون كربن فتوسنتزي (PCA)] واقع شده در انتهاي (D) distal سلول. PC يعني PEP كربوكسيلاسيون و DC يعني دكربوكسيلاسيون اسيد C4 ..b يك سلول مزوفيل فتوسنتزي از Bienertia cyclopteraكه اجزاي داخلي سيتوپلاسمي (PCR) كه برخورد ميكندبا كانالهاي سيتوپلاسمي (CC) به سمت سيتوپلاسم سطحي را نشان ميدهد. روبسيكو و در كروپلاست در بخش مركزي مستقر شده است [با رنگ قرمز نشان داده ميشود] اطرافش را واكوئل v )) قرار گرفته است، سيكلهاي C4 براي هردوگونه در جايي كه PEP كربوكسيلاسيون شكل اسيد C4 رار در ناحیه PCA نشان می دهد ، مشخص شده است. اين هادر ناحيه PCR دكربوكسيله ميشوند و يك اسيد C3 تشكيل ميشود و CO2 آزاد ميشود.
فتوسنتز C4 در يك سلول در گياهان خاكي
فتوسنتز C4 در يك سلول در سيستم گياهان خاكي ابتدا در B. aralocaspica يك Semi-succulent از اعضاي خانواده Chenopodiaceae (suadeae → نژاد salsoloidea زير خانواده) در بيابانهاي Salin در مركز آسيا مشخص شد ( 20 ).
از نظر اكولوژي، B. aralocaspica يك هالوفيت گسترده به فرم mono specific ميباشد كه در حاشيههاي بي دوام در یاچههاي نمكي قرار گرفته است. از نظر ظاهري آناتومي داخلي، ساختار كرانز B. aralocaspica ، شبيه به تيپ Salsoloid ميباشد كه معمولاً در salsoloideae ديده ميشود. در مشاهده دقيق هيچ ديوارةجدا كننده Periclinal بين ناحيه PCR و PCA ديده نميشود، B. aralocaspica با كربن ايزوتوپ نشان داده متابوليسم C4 را نشان ميدهد. فتوسنتز CAM هم ميتواند اثرات ايزوتوپيها C4 را نشان دهد ولي در برگهاي گوشتي صورت ميگيرد ( 20 ).
Elena Voznesenskaya و همكارانش به طور صريح فتوسنتز C4 در تك سلول را در گياه B. aralocaspica نشان دادند. در سلولهاي فتوسنتزي B. aralocaspica تغييراتي صورت گرفت است كه باعث جدايي عملكرد PCR و PCA به همان طريقي كه در بافت كرانز صورت ميگيرد، شده است به جاي اينكه در سلولهاي مختلف انجام گيرد، PCR و PCA در دو انتهاي مقابل يكديگر در يك سلول طويل شده صورت ميگيرد (شكل a6). بازسازي فسفوانول پيروات در كلروپلاستهاي واقع شده در انتهاي distal سلول دور از دستجات آوندي صورت ميگيرد. در حاليكه عمل PCR و روبسيكو در انتهاي proximal سلول، نزديك به دستجات آوندي واقع شده است. در برگ، سلولهاي فتوسنتزي اطراف استوانه مركزي از سلولهاي ذخيره اي آب طويل شده و تعداد زيادي دستجات آوندي تشكيل شده مرتب شده است. انتهاي پروكسيمال سلولهاي فتوسنتزي به صورت محكم نه به صورت مشخص به فضاي بين سلول بسته شده است. در حاليكه در انتهاي distal به طور مشخص نمايان است. فسفوانول پيرات كربوكسيلاز (PEPCase) در سطح بيروني سلولها متمركز نشده است ولي به طور كامل در سیتوپلاسم يافت شده است. اين يافته ها كه جدايي متابوليسمي PCR و PCA را بيان ميكند شامل اجزاء فسفوانول پيرات كربوكسيلاز PEPcase نيست، اما در عوض تمركز آنزيمهاي PPDK (pyruval, phosphate dikinase) ، روبسيكو و آنزيمهاي دكربوكسيلاسيون را شامل ميشود. ميزان كربن ايزوتوپ در B. aralocaspica در بين گياهان C4 خوب است و اين مطلب نشان ميدهد كه كه تراوش (نشت) CO2 پايين است. نشت CO2 به وسيله آرايش شعاعي سلولهاي فتوسنتزي طويل شده به حداقل رسيده است، زيرا يك راه انتشاري طولاني را براي خروج CO2 بايد طي كند. به علاوه تغييرات ساختماني، حالت بيوشيميايي آنزيمهاي PCR و PCA سبب ايجاد راهي براي كاهش نشت ميباشد. B. aralocaspicar ، فعاليت روبسيکو نسبت به فعاليت PPDK (pyruval, phosphate dikinase) دو برابر است كه وابستگي آن را به گونههاي ((salsola laricina نشان ميدهد. بنابراين، نسبت فعاليت فسفوانول پيرات كربوكسيلاز PEPCase به روبسيكو در S. laricina نزديك به 18 است در حاليكه در B. aralocaspica تقريباً 6 است. فكرمي شد كه اين نسبت پايه در B. aralocaspica (كه نياز به PEPCase فسفوانول پيرات كربوكسيلاز جهت جبران نسبت CO2 خارج از داخل سلول دارد ) بيشتر باشد. این نوع کشیده شدن در گیاه به وسیله سیتواسکلتون یعنی رشته های اکتین و میکروتوبولی صورت می گیرد ( 3 ، 20 ).
به طور جالب آنزيمهاي دكربوكسيلاسیون در B. aralocaspica فعاليت پاييني داشتند. جمع فعاليت آنزيمهاي NAD-malic 25 % از آن چيزي بود كه در S.laricina مشاهده شد. در سيستم C4 تك سلولي در B. aralocaspica به نظر ميرسد كه تغيير حالت آنزيمهاي PCR و PCA تا اين حد كه جايگاه CO2 روبسيكو در ناحيه پروكسيمال سلول است باعث افزايش وابستگي اين سيستم به فعاليت سيكل C4 شده است به عنوان دليل، به طور نسبي بيشتر CO2 اي كه پمپ ميشود، ميتواند خيلي سريع قبل از اينكه خارج شود (نشت كند)، تثبيت شود. به علاوه، سطح CO2 اطراف روبسيكو ممكن است كمتر از بيشتر انواع گونههاي گياهي يا فتوسنتز C4 باشد، بنابراين شيب غلظت CO2 نشتي كاهش مييابد. به طور ثابت B. aralocaspica نقطه اشباع CO2 بالاتري نسبت به S. laricina دارد. شيب اوليه منحني CO2 فتوسنتزي كه نيروي پمپ CO2 را نشان ميدهد، در B. aralocaspica نسبت به S. laricina كاهش مييابد (20).
كشف سيستم فتوسنتزي C4 در يك سلول در گياه B. aralocaspica تحقيقات را به سمت گونه Bienertia cycloptera (از نژاد suacdeae) كه در زيستگاههاي نمكي وسيعي در مركز آسيا رشد ميكند، هدايت كرد. Bi.cycloptera يك گياه منحصر به فرد است زيرا اثرات فتوسنتزي C4 را نشان ميدهد ولي در عين حال طبق مطالعات بيوشيميايي قديمي تر جز گياهان C3 شناخته شده بود. Bi. cycloptera يكي از جالب ترين گونههاي C4 مطالعه شده در اين زمان ميباشد. اين گياه مسير فتوسنتزي C4 را در يك سلول انجام ميدهد با استفاده از يك آرايش سلولي جديد كه به طور مشخص از گونه B. aralocaspica و ساير گونههاي C4 متفاوت ميباشد. (شكل b6). به جاي اينكه سلول كشيده شود تا عملكرد PCR و PCA از هم جدا شود،
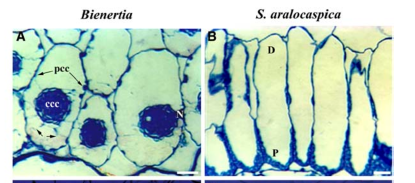
شکل : آناتومی سلوسی کلرانشیم S. aralocaspica و Bienertia . A. برش عرضی برگ Bienertia سیتوپلاسم به دو بخش CCC و PCC تقسیم شده است. فلش های کوچک نشان دهنده کانال های سیتوپلاسمی می باشد. B. برش عرضی از کلرانشیم S. aralocaspica . به وسیله ارگانل ها به دو بخش D و P تقسیم شده است.
Suaedeae و تكامل فتوسنتز C4
با كشف دوگونه از نژاد Suaedeae كه در يك سلول به صورت C4 فتوسنتز ميكنند، اين نژاد به عنوان يكي از جالب ترين گروهها در بين زيست شناسان گياهان C4 قرار گرفت. Suaedeae شامل 4 جنس است:
1) Suaeda ( 100گونه، 60% C4)
2) Alexandra ( 1 گونه C3).
3) Bienertia ( 1 گونه C4).
4) Borszczowa ( 1 گونه C4).
حدس زده ميشود كه نژاد suaedeae داراي 5 منشأ مختلف براي سيستم C4 باشد: 3 تا در Suaeda و يكي در Bienertia ديگري در Borszczowia مشاهده ميشود. چرا Suaedeae تا اين حد در فتوسنتز C4 توسعه يافته است؟ احتمالاً گستردگي خاكهاي نمكي كه گونههاي suaedeae بر روري آن رشد ميكنند، علت اين توسعه باشد. نمك بالا، رقابت بين گونه اي را محدود ميكنند و صفات مشخصه اي را كه سبب استفاده مؤثر از آب ميشود را ايجاد ميشود. بنابراين صفات خاص تازه اي كه استفاده موثر از آب را بهبود بخشد، مثل فتوسنتز C4 در يك سلول شايد كه رقابت كننده فضاي ازاد به سري تكامل باشد. جالب اين جاست كه در سالهاي اخير، محصولات C3 مثل برنج به سمت گياهان C4 چرخيدهاند. بزرگترين مانع براي جلوگيري از تبديل گونههاي C3 به C4 علت بيوشيميايي ندارد بلكه به علل ساختاري است. گونههاي C3 به آنزيمهاي موردنياز جهت فتوسنتز C4 مجهز ميباشند. و حتي بعضي از آنها مثل كرفس و تنباكو، نسخه اي از سيكل C4 را در ريشهها و سلول های پارانشيمي آوندي در ساقههاي فتوسنتز كننده انجام ميدهند. مانع مهمتر، وجود ساختارهاي كرانز در برگ ميباشد كه جهت غلظت CO2 ميباشد. با اكتشاف فتوسنتز C4 در يك سلول، اين كار در طراحي گياهان C4 نسبت به گياهان C3 ، آسانتر از آن چيزي است كه قبلاً تصور ميشد. زيرا اين گونهها چگونگي انجام فتوسنتز در يك سلول را نشان ميدهد. گياهان بياباني گمنام مثل Brorszczowia و Bienertia شايد كليد شناسايي مسير C4 به سمت محصولات C3 باشد ( 20 )

آناتومی ، بیوشیمی و فیزیولوژی برگ هایPhragmites
فعالیت آنزیم اصلی که در متابولیسم کربن درگیر است ، یعنی ریبولوز 1 و 5 بیس فسفات کربوکسیلاز / اکسیژناز ( روبیسکو ) ، تحت شرایط محیطی بالاتر است ( µmol/ms 59.8 و 64,2 به ترتیب در برگ های بالغ و جوان ) . بر عکس ، فعالیت فسفو انول پیروات کربوکسیلاز هم در برگ های بالغ و هم دربرگ های جوان پایین است ( به ترتیب 8.1 , 7.8 ) ( علی رغم فعالیت بالای روبیسکو ) ، میزان فتوسنتز برگ های Phragmites در Leaf area basis پایین است( 1).
وابستگي رشد، تكوين و فتوسنتز به دما در ذرت تحت شرايط CO2 بالا رفته غلظت CO2 اتمسفر عمومي (Ca) در حال افزايش است (367µ molmol-1 in 1999) و تصور ميشود در انتهاي قرن 21 بهµ molmol-1 540 تا 970 برسد.طرح های مدلي اخير براي آب و هوا پيشنهاد ميدهد كه دماي هواي سطحي عمومي، C°4/1 تا 8/5 همراه با دو برابر شدن غلظت CO2 اتمسفر عمومي (Ca) ، افزايش مييابد. چون هم دما و هم غلظت CO2 از مهمترين تغييرات محيطي در فرآيندهاي فيزيولوژيكي و فنولوژيكي (مطالعه آب و هوا و پديدههاي زيست شناسي) در گياهان ميباشد، بنابراين سنجش تأثيرات غلظت CO2 عمومي و دماي هوا بر روي رشد و بازده محصولات گياهي يك مسئله مهم و بحراني ميباشد. زيرا تغييرات دما و غلظت عمومي CO2 به همراه يكديگر اتفاق ميافتد، تعيين بر همكنشهاي اين دو متغير آب و هوايي جالب ميباشد( 4 ، 10).
در گياهان C3 ، به طور عمومي افزايش رشد و فتوسنتز در پاسخ به زياد شدن غلظت عمومي CO2 ديده ميشود. با اين حال پاسخ های گياهان براي اعتدال افزايش غلظت عمومي CO2 مكانيسمهاي مختلفي دارد كه در جهت خو گرفتن گياه به آب و هواي جديد صورت ميگيرد. به علت اختصاصات آناتومي و بيوشيميايي كه در گياهان C4 در جهت مكانيسمهاي تغليظ CO2 صورت ميگيرد، تصور ميشد كه پاسخ هاي رشد و فتوسنتز به افزايش غلظت عمومي CO2 در اين گياهان حداقل باشد. ولي مطالعات گوناگون گزارش داد كه فتوسنتز و رشد در گونههاي C4 پاسخ مثبتي را به افزايش غلظت عمومي CO2 نشان داده است. به طور عمومي، گياهان C4 دماي اپتيموم بالاتري براي رشد و فتوسنتز نسبت به گياهان C3 دارند. بنابراين جهت زندگي در آب و هواهاي گرمتر، بهتر سازگار شدهاند. اين مطلب هنوز نامشخص است كه آيا رشد و فتوسنتز وابسته به دما در گياهان C4 در شرايطي كه غلظت عمومي CO2 افزايش يافته، نسبت به غلظت عمومي CO2 حال حاضر، باز هم بدون تغيير باقي ميماند؟ در گياهان C3 ، دماي اپتيموم براي فتوسنتز در شرايط افزايش غلظت C3 اتمسفر عمومي (Ca) ، بيشتر از شرايط كنوني است، و خاصيت تحريك كنندگي فتوسنتز توسط غلظت CO2 اتمسفر عمومي (Ca) بالا، در دماي بالاتر، بيشتر ميشود. ممكن است تأثيرات متقابل CO2 و دما بر روي رشد و فتوسنتز در گياهان C4 نيز، مشابه گياهان C3 باشد، اما نياز به آزمايشات بيشتري است ( 8 ، 9 ، 10 ).
در Amaranthus ، نقطه اشباع CO2 در دماي تعيين شده اي كه در آن فتوسنتز به CO2 حساس است، افزايش پيدا كرد، ممكن است در گياهان C4 با دماي بالاتري افزايش پيدا بكند. فتوسنتز وابسته به دما در Ca پایین (<36)Pa مشابه به گياهان C3 مثل Amaranthus ميباشد. دانستن بر همكنش بين Ca افزايش يافته و دمايهاي بالاتر در گياهان C4 كمك بزرگي جهت پيشبيني پاسخ های گياهان C4 در تغييرات آب و هوايي آينده دارد (10 ).
همچنين، گزارش شده است كه فتوسنتز گياهان C4 نيز در شرايط افزايش CO2 به مدت طولاني، به آب و هواي جديد خو ميگيرد. در مطالعات پيشين، كه ميزان تبادلات گازي برگي را اندازه ميگرفت، كربوكسيلاسيون مؤثر و نرخ فتوسنتزي CO2 اشباع را به خوبي يك احياء در فعاليت يك آنزيم C4 ، در تيمار با افزايش غلظت CO2 اتمسفر عمومي Ca نشان ميدهد. با اين حال، هنوز نامعلوم است كه چگونه سازگاري فتوسنتزي به آب و هوا جديد در غلظت CO2 اتمسفر عمومي بالا در گياهان C4 به دماي رشد ارتباط دارد ( 10 ).
استفاده از سيستم های افزايش CO2 هواي آزاد (FACE) free-air CO2 enrichment وسيله را براي دانشمندان فراهم ميكند تا تأثير Ca افزايش يافته و ساير تغييرات آب و هوايي را در گياهان C4 و C3 در تنظيمات ميداني باز تعيين كنند. با اين حال كنترل دماي هوا در شرايط ميداني مشكلاتي دارد ( 10 ).
تحقيقات خاك – گياه – جو (SPAR)Soil-Ptant-atmosphere research يك متد تناوبي براي مطالعه تأثيرات متقابل Ca و دماي هوا بر روي رشد گياه فراهم ميكند. زيرا اين متد ميتواند دماي هوا و رطوبت را تحت شرايط طبيعي نور خورشيد كنترل كند. توانايي واحدهاي SPAR در سنجش زمان واقعي تبادل گاز برگها در حين كنترل دماي هوا و غلظت CO2 رطوبت، تعيين دمای فرایند های فيزيولوژيكي را تحت شرایط Ca افزایش یافته در يك بازه وسیعی از دمای رشد ، امکان پذیر می سازد ( 10 ).
ذرت بیشترین گیاه C4 کشت شده در دنیا است . يک برآورد دقیق از تاثیرات Ca و دمای افزوده شده بر روی رشد و نمو گیاه حساس است . زیرا می توان تغییرات بی سابقه و شدید آب و هوا را بر روی بازدهی ذرت پیش بینی کرد . تاثیرات متقابل Ca و دما بر روی رشد و فتوسنتز برای بسیاری از گیاهان C3 مثل محصولات عظیم برنج ، سویا ، گندم بررسی شده است. هیچ نمونه ای از یک گیاه C4 به خصوص ذرت وجود نداشته است. در یک استدلال ابتدایی برای بیان اثرات متقابل Ca بالا و دمای بالا رفته بر روی رشد و فتوسنتز در گیاهان C3 متوجه می شویم که این امر سبب جلوگیری از تنفس نوری به وسیله Ca بالا می شود. که در نتیجه فتوسنتز به طور متوالی در دماهای بالاتر افزایش می یابد( 10 ).
علی رغم گیاهان C3 در گیاهان C4 تنفس نوری پایین است زیرا این گیاهان از مکانیسم تغلیظ CO2 استفاده می کنند. این مسئله نشان می دهد که Ca افزایش یافته ، رشد و فتوسنتز وابسته به دما را به طور معنی داری تغییر نمی دهد. مگر این که در سیکل C4 ، دما به طور قابل ملاحظه ای تغییر بکند. تعریف و توصيف فرآیندهای فنولوژیکالی و فیزیولوژی بر روی محصولات کشاورزی در Ca کنونی و افزایش یافته ، کلیدی در جهت پیش بینی پاسخ های سیستم های کشاورزی و تولیدات آن در تغییرات آب و هوایی جهانی می باشد ( 10 ).
نتیجه : رشد ، نمو و فتوسنتز ذرت در پاسخ به CO2 افزایش یافته تغییر نکرد ولی به طور معنی داری به وسیله دمای افزایش یافته تغییر کرد. همچنین ، دمای وابسته به پارامترهای رشد ، نمو و فتوسنتز به طور معنی داری به وسیله CO2 افزایش یافته تغییر نکرد. دمای اپتیموم برای Am برگی و نرخ ظاهری برگی نزدیک به 34 و 31 درجه سانتی گراد بود. کربوکسیلاسیون موثر و Vmax تخمین زده شده برای منحنی های A / ci برگی در پاسخ به CO2افزایش یافته در مقابل دما کاهش یافته است. فعاليت آنزيمهاي C4 در invitro كاهش يافت اين نتايج معلوم ميكند كه در حالي كه بسياري از پارامترهاي رشد و فتوسنتز در اين جا آزموده شود ولي كمترين تأثيرپذيري را در شرايط Ca افزوده شده مشاهده كرديم. فرآيندهاي سازگاري به آب و هواي جديد در سيكل C4 به وسيله كاهش فعاليت آنزيمهاي C4 رخ ميدهد ( 10 ).
تاثیر سالیسیک اسید بر روی اثرات کادمیوم
کادمیوم یک عنصر بسیار خطرناک است که توسط فرایندهای صنعتی و کودهای فسفاته وارد محیط زیست شده است. این عنصر در خاک های کشاورزی می تواند به سطح بالایی برسد و به راحتی توسط گیاهان اسیمیله می شود. وقتی این عنصر توسط گیاهان جذب می شود ، اثرات نامطلوبی را بر روی گیاهان می گذارد : مثل لوله شدن برگ ، کلروریز ( زرد یا سفید شدن کلروفیل) ، کاهش رشد در ریشه و اندام های هوایی ، قهوه ای شدن نوک ریشه و در نهایت مرگ. موارد دیگر کادمیوم بر روی متابویسم چنین است : کاهش جذب مواد غذایی ، تغییر در متابولیسم نیتروژن و مهار بسته شدن روزنه ها.فتوسنتز هم به طور مستقیم تحت تاثیر کادمیوم قرار می گیزد. زیرا این عنصر بر وی کلروفیل تاثیر می گذارد.تاثیر منفی دیگر کادمیوم در فاز کربوکسیلسیون فتوسنتز است. اهداف اصلی که کادمیوم بر روی آن ها اثر می گذارد ، دو آنزیم اصلی در تثبیت CO2 می باشد. یکی روبیسکو و دیگری فسفوانول پیروات کربوکسیلاز می باشد. یون های کادمیوم فعالیت روبیسکو را به وسیله جانشینی در یون منیزیم کاهش می دهد. و فعالیت روبیسکو را به سمت واکنش های اکسیژنازی تغییر می دهند ( 11 ).
سالیسیلیک اسید یک مولکول سیگنالی توانا در گیاهان است که در پاسخ های ویژه به استرس های زیستی و غیر زیستی در گیر می باشد. نشان داده شده است که سالیسیلیک اسید محافظتی را در برابر کاهش دما در گیاه ذرت و گیاهان گندم زمستانه فراهم می کند.و همچنین پاسخ های گیاه را به استرس های اسمزی ، نمکی و پاتوژنی تغییر می دهد . به عتاوه در حفاظت گیاه در برابر فلز های سنگین نقش دارد. مشاهده شده است که تیمار با سالیسیلیک اسید تاثیر کادمیوم را در فتوسنتز گیاهان ذرت کاهش می دهد ( 11 ).
منابع
1. Antonielli M. et al. ( 2002 ). Physiological & anatomical characterization of Phragmites australis Leaves. Aquatic Botany. 72. 55 – 66. www.elsevier.com/locate/aquabot.
2. Chastain. C.J. et al. ( 2003 ). Regulation of pyruvate , Orthophosphate Dikinase by ADP -/Dependent reversible Phosphorylation in C3 & C4 Plants. Plant Physiology & Biochemistry. 41. 523 – 532. www. .elsevier.com/locate/plaphy
3. Chuong S.D.X. et al. ( 2006 ). The Cytoskeleton maintains Organelle Partitioning Required for single – Cell C4 Photosynthesis in Chenopodiacea species. The Plant Cell. 18. 2207 – 2223. www.plantcell.org
4. Crafts S.J. et al. ( 2004 ). Analyzing the Impact of High Temperature & CO2 on Net Photosynthesis : Biochemical Mechanisms , Models & Genomics. Field Crops Research. 90. 75 – 85. www.elsevier.com/locate/fcr
5. Foyer C.H. et al. ( 2002 ). Regulation of Photosynthesis & Antioxidant in Maize Leaves at Optimal & Chilling Temperatures : Review. Plant Physiology & Biochemistry. 40. 659 – 668. www. .elsevier.com/locate/plaphy
6. Fukayama H. et al. ( 2001 ). Significant Accumulation of C4 – Specific Pyruvate , orthophosphate dikinase in a C3 Plant , Rice. Plant physiol. 127. 1137 – 1146.
7. Gerrard M.C. etal. ( 2005 ). A Comprehensive Analysis of the NADP – Malic Enzyme Gene Family Arabidopsis . Plant Physiology. 139. 39 – 51. www.plantphysiology.org
8. Huang y. etal. ( 2006 ) . Climate & environmental Controls of the Variation of C3 & C4 plant Abundance in Central Florida for the Past 62000 Years. Palaeogeography. 237. 428 – 435. www.elsevier.com/locate/palaeo
9. Keeley J.E. et al. (2003 ). Evolution of CAM & C4 Carbon – Concentrating Mechanisms. Int.J. Plant Sci. 164 ( 3 suppl. ). S55 – S 77.
10. Kim S.H. et al. ( 2007 ). Temperature Dependence of Growth , Development & Photosynthesis in Maize Under Elevated CO2. Enviromental &Experimental Botany. 61. 224 – 236. www.elsevier.com/locate/envexpbot.
11. Krantev A. et al. ( 2006 ). Treatment with Salicylic Acid decreases the Effect of Cadmium on Photosynthesis in Maize Plants. Plant Physiology. 1 – 12. www.elsevier.de/jplph
12. Lai L.B. et al. ( 2002 ). Differential Regulation of transcripts Encoding cytosolic NADP-Malic Enzyme in C3 & C4 Elaveria Species. Plant Physiology. 128. 140 – 149. www.plantphysiology.org
13. Leegood R.C. et al. ( 2002 ). C4 Photosynthesis : Principles of CO2 Concentration & Prospects for its Introduction into C3 Plants. Experimental Botany. 53. 561-590.
14. Lepiniec L. et al. ( 2003 ). From Enzyme Activity to Plant Biotechnology : 30 Years of Research on Phosphoenol pyruvate Carboxylase. Plant Physiology & Biochemistry. 41. 533-539.www. .elsevier.com/locate/plaphy
15. Maroco J.P. et al. ( 1998 ). Oxygen Requirment & Inhibitin of C4 Photosynthesis An Analysis of C4 Plants Deficient in the C3 & C4 Cycle. Plant Physiol. 116. 823-832.
16. Mastumura H. et al . ( 2002 ). Crystal Structures of C4 From Maiz & Quaternary Complex of E. coli phosphoenolpyruvate Carboxylases . Structure. 10. 1721-1730.
17. Miyao M. et al. ( 2003 ). Molecular evolution & genetic Engineering of C4 photosynthesis Enzyme . Experimental Botany. 54. 179-189.
18. Patel M. et al. ( 2004 ). Untraslatad regions from C4 Amaranth AhRBcS1 mRNAs Confer Translational enhancement & Preferential Bundle Sheath Cell Expression in Transgenic C4 Flaveria bidentis. Plant Physiology. 136. 3550-3561. www.plantphysiology.org
19. Rao S.K. et al. ( 2008 ). Kinetic Analyses of recombinant Isoforms of Phosphoenolpyruvate Carboxylase from Hidrilla verticillata Leaves & the impact of Substituting a C4 – signature Serine. Plant Science. 7815. 1-9. www.elsevier.com/locate/plantsci.
20. Sage R.F. ( 2002 ) C4 Photosynthesis in Terrestial Plants Does not Require Kranz Anatomy. Trends in Plant Science. 7. www.plants.trends.com.
21. Takabayashi A. et al. ( 2005 ). Differential use of two Cyclic electron flow Around Photosystem І from Driving CO2 – Concentration Mechanism in C4 Phptosynthesis. PNAS. 102. 16898-16903. www.pnas.org
22. Ueno O. ( 1998 ). Induction of kranz Anatomy & C4 – like Biochemical Characteristics in a Summerged Amphibious plant by Abcisic Acid.
منبع :
 سلام به این وبلاگ خوش امدید
سلام به این وبلاگ خوش امدید